WAS BEDEUTET WASSERSTOFF DEHYDRIERUNG?
Inhärent sichere Dehydrierung
Dieser Artikel beschreibt den Dehydrierungsprozess, d.h. wie Wasserstoff aus einem festen Wasserstoffsystem entzogen wird.
Bei einem gesättigten Wasserstoffträgermaterial sind die Wasserstoffatome in der Gitterstruktur des Metallhydrids integriert. Wenn Wasserstoff aus dem Speicher entnommen wird, sinkt der Druck um dieses gesättigte Festkörpermaterial, wodurch ein Druckunterschied zwischen dem Plateaudruck des Metallhydrids und dem Druck des umliegenden Gases entsteht. Dieser Unterschied treibt die Wasserstoffatome an der Grenzfläche zwischen dem Festkörper und dem Gas zur Rekombination und zur Bildung von molekularem Wasserstoff (H2). Diese H2-Moleküle gehen dann in die Gasphase über.
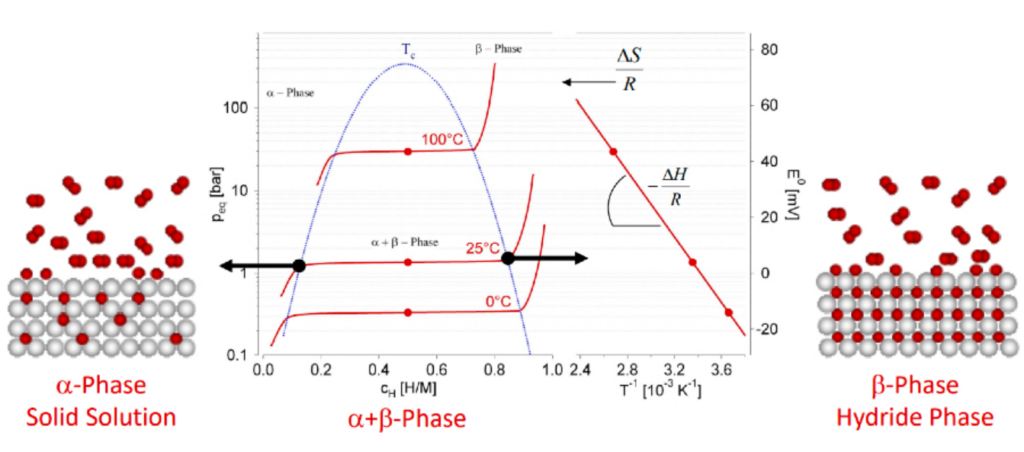
Der Prozess der Wasserstoffrekombination und -freisetzung ist endotherm, d. h. es wird Energie benötigt, um die Wasserstoff-Metall-Bindungen innerhalb des Metallhydridgitters aufzubrechen. Dieser Energiebedarf verdeutlicht die Komplexität und Schwierigkeit des Dehydrierungsprozesses, da er die Aufnahme von Wärme erfordert, um die Freisetzung von Wasserstoffgas zu erleichtern. Die grafische Darstellung in der folgenden Abbildung veranschaulicht dieses Phänomen, indem sie die Phasen der Wasserstofffreisetzung aus dem Metallhydrid und seinen Übergang in die Gasphase zeigt.
Für die Optimierung von Wasserstoffspeichersystemen ist das Verständnis dieses endothermen Prozesses von entscheidender Bedeutung, da er die Effizienz und Geschwindigkeit der Wasserstofffreisetzung beeinflusst. Eine ordnungsgemäße Handhabung der thermischen Dynamik kann die Sicherheit und Leistung dieser Systeme verbessern und eine stabile Versorgung mit Wasserstoffgas bei Bedarf gewährleisten.
Dieses Phänomen tritt auf atomarer Ebene auf und hat weitreichende Auswirkungen auf das makroskopische Verhalten des Systems und seine Sicherheitseigenschaften. Wenn ein Leck auftritt, kann nur ein begrenzter Teil des gespeicherten Wasserstoffs sofort entweichen. Der austretende Wasserstoff kühlt das System rasch ab und bringt es in einen neuen Gleichgewichtszustand. Daraufhin verringert sich die Leckrate und kann letztendlich ganz zum Stillstand kommen. Dies geschieht entweder, weil die lokale Temperatur zu niedrig wird, um die Dehydrierung aufrechtzuerhalten, oder weil die Öffnung, durch die der Wasserstoff entweicht, zufriert. Die folgende Abbildung zeigt ein Speichermodul, aus dem mit einer sehr hohen Durchflussrate Wasserstoff entnommen wurde, was zum Einfrieren des Moduls führte. Dies veranschaulicht den beschriebenen Prozess und zeigt, wie ein schnelles Austreten von Wasserstoff das Gefrieren verursachen kann, wodurch die Öffnung versiegelt und ein weiteres Austreten verhindert werden soll.

Durch Einschränkung bzw. Unterbrechung der Leckströme kann der austretende Wasserstoff schon lange vor Erreichen der unteren Explosionsgrenze des Wasserstoff-Luft-Gemisches erkannt werden. Aufgrund des oben beschriebenen Phänomens ist durch die inhärenten physikalischen Eigenschaften des Systems selbst gewährleistet, dass genügend Zeit zur Verfügung steht, um die Entstehung eines explosionsfähigen Gemisches durch geeignete Maßnahmen zuverlässig zu verhindern. Falls Sie an weiteren Informationen über das thermische Verhalten der Systeme interessiert sind, empfehlen wir Ihnen, auch diesen Artikel zu lesen.